Disolución del NaCl » Recursos educativos digitales

Cloruro de sodio. Estructura de NaCl. Cloruro de sodio. El cloruro de sodio tiene una estructura cúbica cuya celda unidad presenta iones Cl - y Na +. Cada ion Na + tiene un índice de coordinación, (I.C.) igual a seis. La figura muestra tanto los iones que se encuentran dentro de la celda, como los que se encuentran en las aristas.
Átomos y Moléculas, Sustancias Orgánicas

Teoría de la ionización: origen y autoría. La teoría de la ionización es una teoría fundamental en la química y la física que ha sido desarrollada por varios científicos a lo largo del tiempo. Esta teoría se basa en la idea de que los átomos y las moléculas pueden perder o ganar electrones para convertirse en iones cargados.
Enlace iónico características, cómo se forma y ejemplos
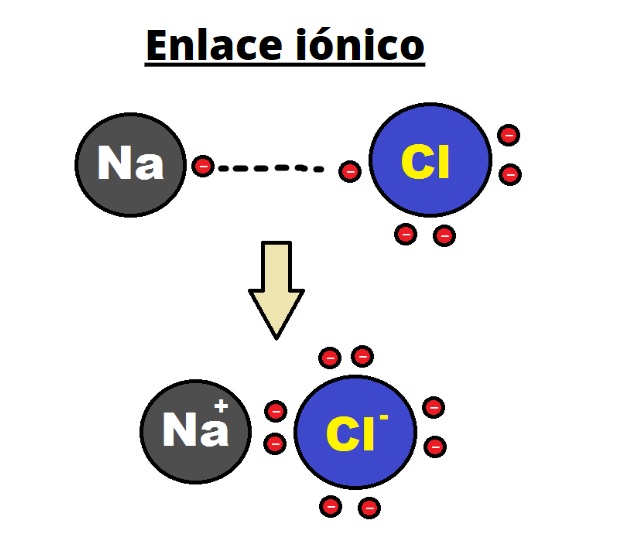
El cloruro de sodio o sal de mesa como se le conoce popularmente, es un compuesto químico formado por un catión sodio (Na +) y un anión cloruro (Cl - ). Este compuesto es producto de una unión o enlace iónico d ebido a la atracción electrostática entre ambos átomos de diferentes cargas eléctricas, donde ocurre una transferencia de.
Clases de Química Enlace ionico y cloruro de sodio
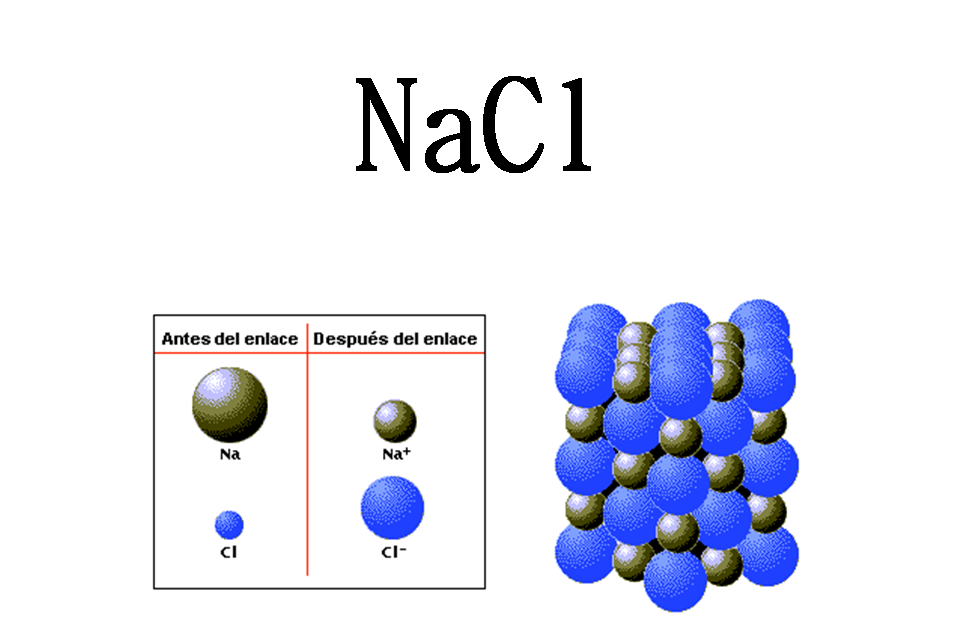
El cloruro de sodio es absolutamente soluble en agua. Por ser un compuesto covalente, el compuesto debe ser insoluble en agua. Por lo tanto, nacl no es covalente en absoluto. Normalmente, la sal de mesa se usa de manera regular en todos los hogares al disolverla en agua. Por lo tanto, esta propiedad iónica básica de la sal nacl es bien.
IONIZACIÓN DE LOS COMPUESTOS QUÍMICOS YouTube

El Cloruro de Sodio, NaCl. El caso clásico de enlace iónico, la molécula de cloruro de sodio, se forma por la ionización de los átomos de sodio y cloro, y la atracción de los iones resultantes. El átomo de sodio tiene 3 electrones fuera de una capa completa, y toma sólo 5,14 electrón voltios de energía, para liberar ese electrón.
Ayuda por favor cual es la estructura de Lewis de NaCL Brainly.lat

El cloruro de sodio (NaCl) es de hecho la unión de un ion Na+ y de un ion Cl- que se atraen mutuamente bajo el efecto de la atracción electrostática. Las moléculas de agua son eléctricamente neutras pero su geometría las hace polarizables, es decir, que las cargas positivas y negativas están colocadas una frente a la otra. Ésta.
iónicos o moleculares?

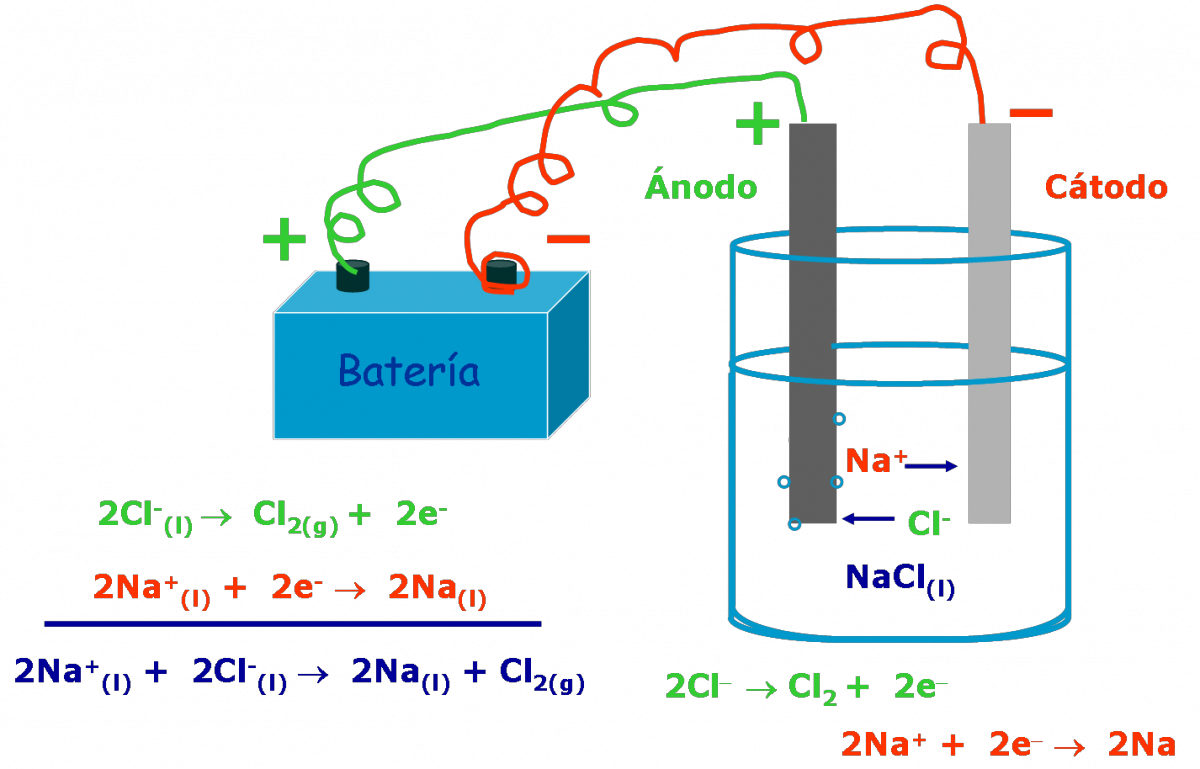
La electrólisis del NaCl ( cloruro de sodio) en fundición se puede realizar en una celda electrolítica común. El electrólito se encuentra formado por una fundición de cloruro de sodio ( con un punto de fusión de 801ºC), que tiene un contenido de iones Na+ y Cl-. Los electrodos, constituidos por lo general de un material inerte como puede ser por ejemplo, el grafito, se encuentran.
Structure of Sodium Chloride (NaCl) Formation of NaCl How to draw NaCl Structure Ionic

Definición. Se denomina enlace iónico al enlace químico de dos o más átomos cuando éstos tienen una diferencia de electronegatividad de 1,7 ó mayor. Este tipo de enlace fue propuesto por W. Kossel en 1916. En una unión de dos átomos por enlace iónico, un electrón abandona el átomo menos electronegativo y pasa a formar parte de la.
¿Cómo se forman los Ácidos, Bases y Sales?
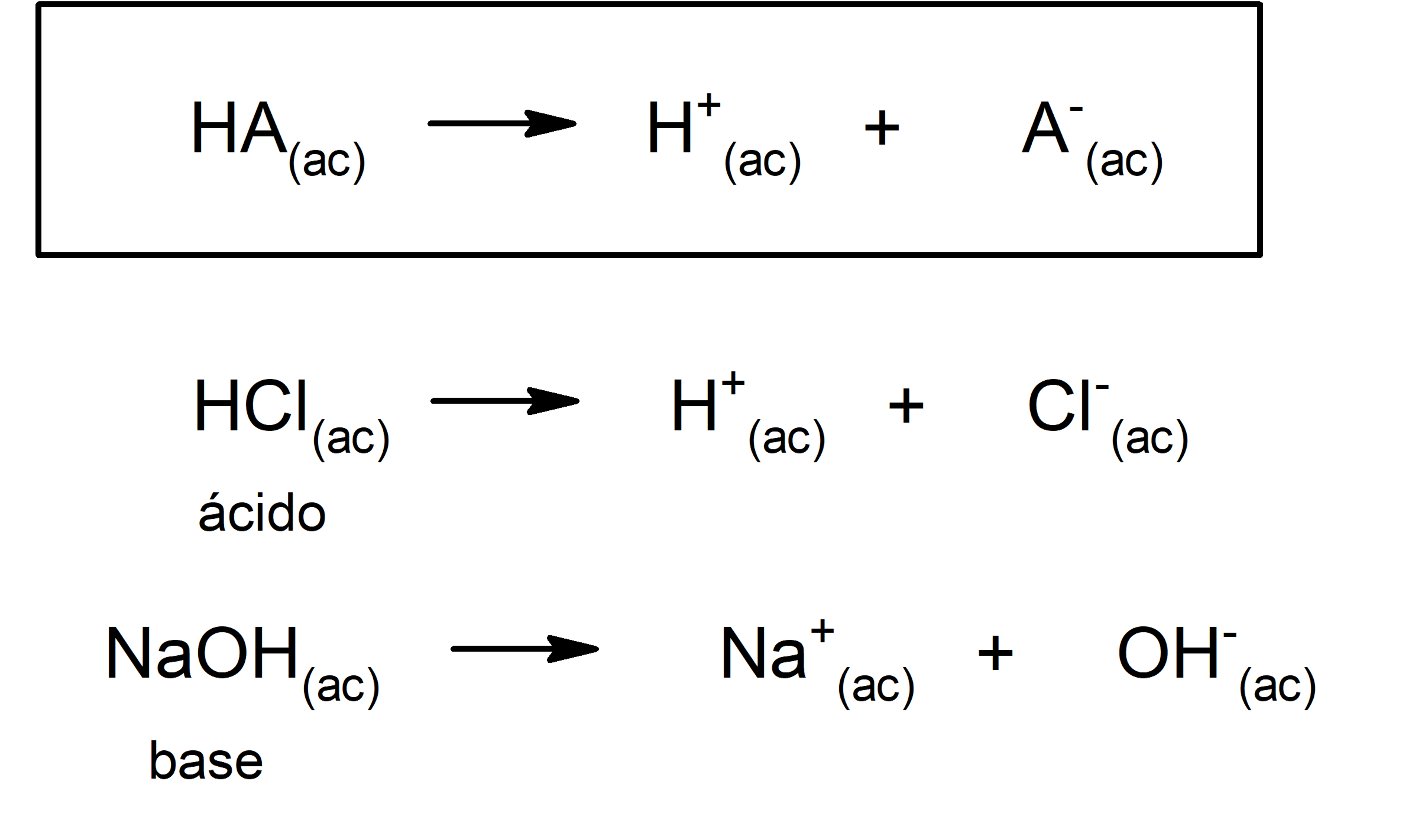
RADIO IONICO. Los radios ionicos aumentan al bajar en un Li+< Na+< K+< Rb+< Cs+. Los radios de los iones de la misma carga disminuyen a lo largo de un período Ca2+>Mg2+>Zn2+ Ca2+ > Ti2+ > V2+. Para iones isolelectronicos los aniones son mayores que los cationes, medida que aumenta la carga nuclear el tamaño disminuye O2- > F- > Na+ > Mg2+ > Al3+.
Química modelo molécula de sal diatomic sodio cloro NaCl elemento científico fórmula. Partículas

El cloruro sódico es la sal mas común, la sal de mesa común utilizada para condimentar los alimentos. Se forma en cristales cúbicos evidente incluso en la sal de mesa. Se presenta comúnmente en forma mineral, la halita, también llamada sal de roca. Se puede formar por la reacción ácido-base del ácido clorhídrico e hidróxido de sodio:
Cómo preparar NaCl 3 (Solución Hipertónica) Fácil YouTube

¿Qué es el enlace iónico y cómo se forma el cloruro de sodio o sal común? En este vídeo, aprenderás los conceptos básicos de los enlaces químicos y verás un ejemplo práctico de cómo se.
Cómo preparar NaCl 0.9 (Cloruro de Sodio) Fácil YouTube

Colegio de Ciencias y Humanidades | Aprender a aprender, aprender a.
Reacción ácidobase neutralización de las propiedades ácido y base, produciendo una sal y agua

5. NaCl: Solubilidad y su relación con el enlace iónico. La sal común, también conocida como cloruro de sodio (NaCl), es un compuesto iónico que se encuentra ampliamente distribuido en la naturaleza y es esencial para la vida humana.
EL FÍSICO LOCO Electrólisis de sales fundidas y disueltas (NaCl)
La formación de iones basada en la regla del octeto se ve fácilmente para el conocido compuesto iónico, cloruro de sodio, NaCl, como se ilustra en la Figura 4.3. Al perder un electrón para convertirse en el catión Na +, la capa subyacente del sodio de 8 electrones se convierte en la capa externa del ion con un octeto estable.
La disolución de NaCl escena en 3D Educación digital y aprendizaje Mozaik
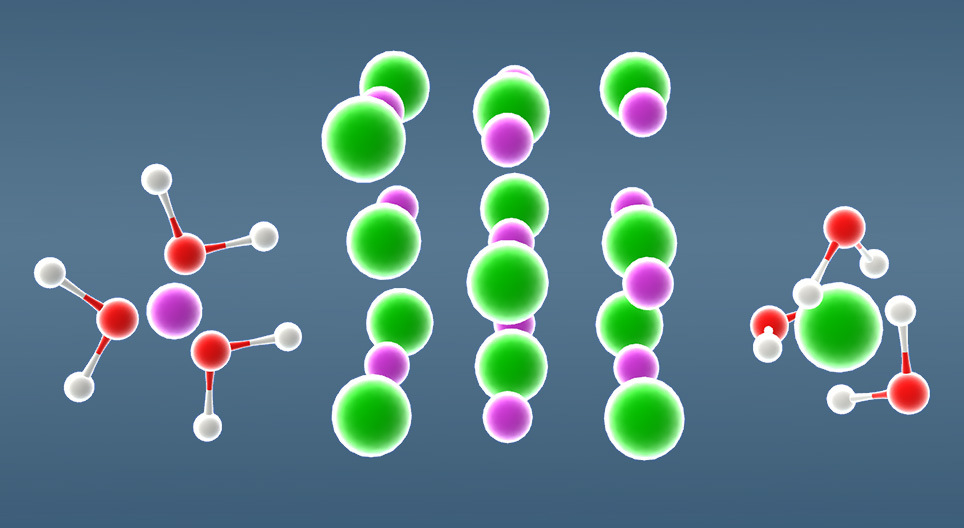
Enlace iónico (diferencia entre 1.7 y 3.3 ) Un enlace iónico se forma cuando los electrones se transfieren completamente de un átomo a otro. Durante este proceso, un átomo pierde electrones y otro los gana, formándose iones. Este fenómeno se presenta entre átomos con diferencias de electronegatividad muy alta (superior o igual a 1.7), el átomo más electronegativo atrae con mayor.
¿Cómo se disuelve el cloruro de sodio (NaCl) en agua? Los iones Na atraen los átomos de oxígeno

4 modelos de enlace en químlca inorgÁnica: 1 . compuestos 112 800 720 640 560 480 400 320 240 80 -80 -160 -240 -320 (g) 495.4 (g) (g) 108.4